Diana L. Walstad "Ecology Of The Planted Aquarium"
В моих аквариумах есть три основных источника питательных веществ: корм для рыб, вода и почва. Я буду сравнивать их, используя один из аквариумов в качестве экспериментального образца. Свое исследование я начала с попытки определить потенциальный дефицит питательных веществ в аквариуме с растениями. В то время я опасалась, что растениям не хватает микроэлементов и что удобрения на их основе стоят дорого и их негде взять.
А. Экспериментальный аквариум и методология
В качестве экспериментального аквариума для своих опытов я выбрала 50 галлонный (~190 л) аквариум с радужницами. Поскольку это аквариум с установившимся биологическим равновесием и со взрослыми рыбами, мне не нужно было беспокоиться о накоплении в нем питательных веществ, выращивая рыб, растения и бактерий, как это было бы в новом аквариуме, где они только начинают работать.
Основным путем утечки питательных веществ из этого аквариума была периодическая (каждые 2 - 3 недели) прополка растений. Не думаю, что другие пути удаления питательных веществ были сколь-нибудь значительными, потому что я стараюсь по минимуму менять воду и чистить аквариум.
Для единообразия и простоты, все данные в этой главе рассчитывались на основе сухого веса и выражены в единицах.
Кормление рыб: в течение недели обычного двухразового кормления рыб, я следила за количеством вносимого корма - за неделю я внесла 9,3 г, что в месяц составляет около 40 г.
Вода и ее подмены: в 50 галлонном (190 л) аквариуме содержится примерно 170 л жесткой воды. (Жесткость воды в моем водопроводе - 137 ppm CaCO3 и GH = 17) Каждые 3 месяца я подменивала около 40% воды, что примерно равно 75 л, в среднем по 25 л в месяц. Плюс доливала еще по 15 л в месяц взамен испарившейся. Таким образом, можно сказать, что в аквариум заливалось в общей сложности 40 л воды в месяц (25 л + 15л)
Почвенный субстрат: на дно аквариума я положила около 10 кг садовой земли слоем 1 дюйм (2,54 см) и засыпала ее 20 - 30 кг гравия слоем 1,5 - 2 дюйма (~ 4 - 5 см).
Прополка растений: я высушила и взвесила все прополотые растения, скопившиеся за 13 недель. Они весили 61 г, что составляет около 20 г в месяц.
Таким образом, в аквариуме было (или вносилось) достаточно питательных веществ для обеспечения 20 г прироста растений каждый месяц. Чтобы рассчитать, сколько каждого элемента было в 20 г, я воспользовалась методом минимальной концентрации элемента, которая, как ожидается, обнаружится в высушенных растениях. Такая концентрация называется критической концентрацией элемента (подробней о методе ниже). Поскольку растения могут накапливать излишки питательных веществ, то в моих растениях концентрация каждого элемента неизменно превышала критическую. Однако последующие свои расчеты питания растений я хотела бы базировать только на необходимых питательных веществах, а не на излишках, которые они накопили в своих тканях произвольным образом. В таблице показано количество каждого элемента, которое требуется моим растениям для обеспечения прироста массы, равного 20 г (сухого веса):
Табл V-1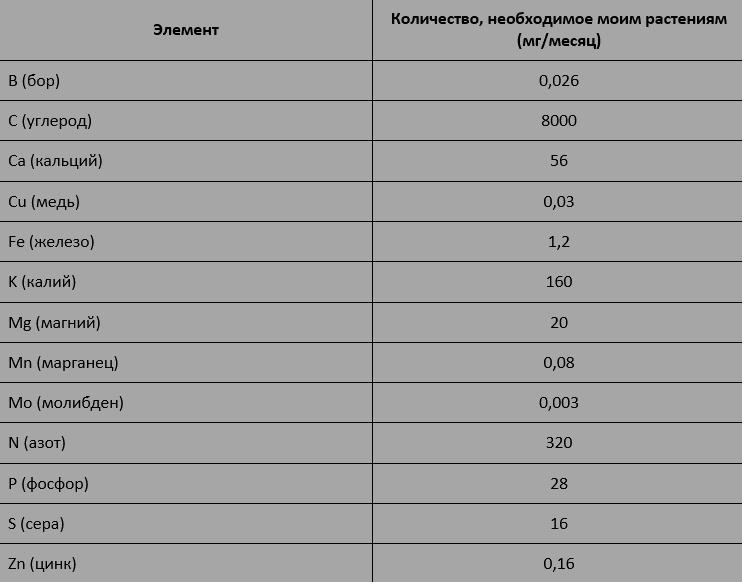 Значения количества, указанные в таблице, были получены путем деления критических значений концентраций элементов для Elodea occidentaiis на 50 (20 г составляет 1/50 кг). Значение C, равное 8000, основано на фактических данных о том, что водные растения состоят на 40% из углерода [1], то есть содержат 400000 мг C/кг сухого веса растения.
Значения количества, указанные в таблице, были получены путем деления критических значений концентраций элементов для Elodea occidentaiis на 50 (20 г составляет 1/50 кг). Значение C, равное 8000, основано на фактических данных о том, что водные растения состоят на 40% из углерода [1], то есть содержат 400000 мг C/кг сухого веса растения.
Б. Рыбий корм
Весь корм, который я даю рыбам, живой ли он, сухой или замороженный, в любом случае состоит из биологических организмов или частей биологических организмов (пророщенные зерна пшеницы, крабовые палочки и т.д.), а не из пластмассы или каких-либо других неорганических элементов. А поскольку все организмы имеют общий химический состав и сходную потребность в определенных элементах, то корм для рыб несомненно содержит все питательные вещества, в которых нуждаются растения.
1. Химическое единообразие живых существ
Учитывая то, что живые организмы колоссально отличаются друг от друга по внешнему виду и поведению, их химическое единообразие просто поражает. Поскольку процессы, лежащие в основе жизнедеятельности организмов одинаковы, то и концентрации химических элементов в них также одинаковы [2]. Например, рыбы, растения, грибы и черви хотя и выглядят совершенно по-разному, но все они содержат около 40-50% углерода. А из 17 элементов, необходимых растениям, только бор не требуется животным, бактериям, водорослям, беспозвоночным и грибкам [3, 4].
Причина такой химической однородности заключается в том, что для всех живых организмов одни и те же элементы более полезны, чем другие. Углерод (C) идеально подходит для создания конструкций. Подобно элементам конструктора, атомы углерода могут соединяться друг с другом, образуя бесконечное разнообразие размеров и форм. А поскольку ни один из более чем 100 элементов на планете не может так делать, то углерод здесь вне конкуренции. Средняя концентрация углерода в организмах составляет около 430000 мг/кг или 43% [1, 5].
Если углерод идеально подходит для изготовления конструкций, то другие элементы, такие как железо и цинк, являются более подходящими элементами для обеспечения функционирования этих конструкций. Клетки всех живых существ, будь то бактерии или клетки, из которых состоят растения и рыбы, должны быстро и эффективно перемещать электроны. Действительно, клеточный метаболизм всех организмов основан на извлечении энергии из движения электронов. Оказалось, что железо и цинк обладают атомными свойствами, необходимыми для эффективного захвата и высвобождения электронов. Напротив, другие металлы, такие как никель и алюминий, слишком медленны и поэтому бесполезны [6]. Вот так и получилось, что железо и цинк используются всеми организмами, тогда как другие элементы используются редко (никель), либо вообще не используются (алюминий).
В таблице показаны концентрации химических элементов в различных готовых кормах для рыб и в живом корме:
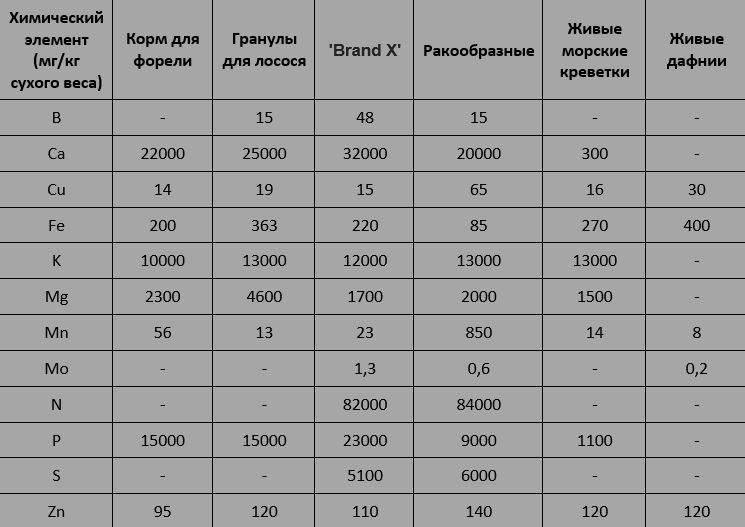
Цифры по корму для форели были взяты из анализа минералогического состава
38 кормов европейских производителей [7]. Гранулы для лосося представляют собой среднее из 12 различных составов для выращивания лосося в штате Орегон [8]. 'Brand Х' - гипотетический корм для рыб. Как и большинство настоящих кормов для рыб, полагаю, что он мог бы состоять на 50% из рыбопродуктов и на 50% из белка с высоким содержанием растительных веществ. Что касается рыбной составляющей, то я усреднила элементный состав 6 - 9 различных рыб по данным НАН (Национальной академии наук) [9]. Для элементов (В, К, Мо, N, S), не включенных в анализ тканей рыб, я использовала данные по морской рыбе [10]. Для растительной составляющей я усреднила значения НАН по элементному составу соевых бобов и дрожжей. Опять же, для элементов, отсутствующих в данных НАН (В, К, Мо, N, S), я использовала данные по древесным покрытосеменным растениям [11]. Наконец, я усреднила значения рыбных и растительных веществ, и получила вышеуказанные цифры для типичного аквариумного корма (например, «Бренд Х»).
Значения по ракообразным - это средние значения в широких пределах [10]. Данные по морским креветкам взяты из исследований науплий [12]. Значения по дафниям взяты из исследования конкретного вида Daphnia pulex [13].
Гранулы для лосося и «Бренд Х» не были дополнены минералами, состав корма для форели не описан.
Все 6 представленных в таблице кормов являют собой либо живые организмы, либо продукты из живых организмов. В таблице можно заметить большой разброс концентрации элементов между разными кормами. Такой разброс отражает количество питательных веществ в окружающей среде организма, но не его потребности. (Организмы часто накапливают больше питательных веществ, чем им необходимо.) Важно то, что эти значения должны быть выше потребностей организма, иначе он не прожил бы достаточно долго, чтобы стать пищей для рыб.
Единственные реальные различия в концентрациях и составе химических элементов между организмами - это меньшее количество азота (N) и серы (S) в растениях по сравнению с животными. Продуценты (растения и водоросли) содержат 3% N и 0,5% S, в то время как хищники (животные, рыбы, беспозвоночные и т. д.) содержат примерно в три раза больше (10% N и 1,3% S) [5]. За исключением хищников, у которых в тканях содержится больше белка, все организмы имеют одинаковые потребности в элементах и, следовательно, имеют одинаковый потенциал (в качестве ингредиента корма для рыб) для обеспечения растений питательными веществами.
2. Корм для рыб в качестве источника питательных веществ
Все рыбные корма содержат элементы, необходимые растениям. Вопрос в том, достаточно ли их? В таблице ниже показаны накопления химических элементов, вносимых вместе с 40 г корма в месяц, дающего 20 г прироста сухого веса растений. Углерод - это питательное вещество, которое меньше всего содержится в рыбных кормах. В экспериментальном аквариуме рыбий корм обеспечивал всего лишь двухмесячный его запас. (Для сравнения: рыбий корм дает 80-ти месячный запас микроэлемента марганца)
Аквариумисты могут использовать метод десятикратного избытка азота для измерения относительного количества питательных веществ, полученных из других рыбьих кормов. Например, если в аквариуме есть избыток азота, значит должен быть и избыток бора. Это связано с тем, что поступление бора из рыбьих кормов (40 месяцев) в четыре раза больше, чем поступление азота за 10 месяцев.
в рыбьем корме
(мг/кг)
веществ
(месяцев)
| Элемент |
Среднее значение
в рыбьем корме
(мг/кг)
|
Запас питательных
веществ
(месяцев)
|
| B |
26 |
40 |
| C |
430000 |
2 |
| Ca |
20000 |
14 |
| Cu |
27 |
36 |
| Fe |
260 |
9 |
| K |
12000 |
3 |
| Mg |
2400 |
5 |
| Mn |
160 |
80 |
| Mo |
0.7 |
9 |
| N |
83000 |
10 |
| P |
13000 |
19 |
| S |
5600 |
14 |
| Zn |
120 |
30 |
Запасы питательных веществ в рыбьем корме для роста растений.
*Среднее значение я вычислила путем усреднения элементов каждого из 6-ти кормов из предыдущей таблицы. Покажу на примере бора, как я вычислила "Запас питательных веществ". Так как 1 кг рыбьего корма содержит 26 мг B, то 0.040 кг (40 г) рыбьего корма, которые я даю в месяц, содержит 1.04 мг бора (0.04 * 26 мг/кг). 20 г растений, которые выросли за этот месяц, содержат минимум 0.026 мг бора. 1.04 мг входящего бария, поделенное на 0.026 будет равно 40. Теоретически, это означает, что 40 г рыбьего корма обеспечивает растения бором на 40 месяцев.
3. Переход питательных веществ из рыбьего корма в аквариумные растения
Химические элементы попадают в рыбу лишь на время. Все здоровые взрослые животные регулируют поступление питательных веществ в свой организм с помощью механизмов гомеостатического контроля, чтобы необходимые элементы не накапливались до токсичных уровней [14].
Таким образом, по мере того как рыба извлекает энергию из крупных органических соединений корма, она выделяет продукты распада, небольшие неорганические соединения, которые могут использоваться растениями. Например, N, S и C, содержащиеся в белках рыбьих кормов, будут преобразованы в аммиак, сульфаты и углекислый газ, которые могут быть немедленно поглощены листьями растений. И все, что рыба не съест либо выделит, перерабатывается бактериями практически таким же образом.
Вот почему организмы, будь то бактерии, рыбы или человек, используют одинаковые механизмы обмена веществ для извлечения энергии из пищи. (По сути, метаболизм - это просто обратный процесс фотосинтеза.)
*То, что может показаться исключением из вышеперечисленного, является просто вариациями этой объединяющей темы. Например, не смотря на то, что растения готовят себе пищу, используя свет, а хемоавтотрофные бактерии готовят себе пищу, используя химическую энергию, перерабатывают они ее точно так же, как это делают животные. А в отсутствие кислорода некоторые бактерии могут использовать другие акцепторы электронов во время метаболизма. Однако механизм генерации энергии (образование АТФ в результате переноса электронов) тот же самый.
По мере потребления органических соединений (таких как глюкоза) и кислорода, выделяются углекислый газ, вода и энергия.
C6 H12 O6 + 6O2 => 6CO2 + 6H2O + энергия
С биологическим циклом аквариума связано множество чисто химических циклов: солюбилизация, выпадение в осадок, связывание и высвобождение химических элементов. Однако сами элементы остаются неизменными. То есть железо, содержащееся в живых креветках, которых поймали, высушили, перетерли в муку, которую спрессовали в таблетки, такое же самое, как если бы оно было добавлено в аквариум, как компонент живых креветок. Химические элементы стабильны "как скала".
Некоторые химические элементы выводятся организмом рыб прямо в воду, где их тут же легко могут усваивать растения. (Рыбы выделяют большинство переваренных химических элементов B, K, Mg, Mo, N, S и C в виде водорастворимых соединений с мочой или через жабры.)
Другие элементы напротив, выводятся рыбами, как правило в твердом виде. Большая часть кальция и фосфора, которые содержатся в корме, будет выведена рыбой в твердом виде с экскрементами.
Металлы Cu, Fe, Mn и Zn будут даже менее доступны для растений, чем Ca и P, потому что очень мало этих элементов выводится в жидом виде с мочой или через жабры.
* Например, 97% азота, 94% серы, 64% фосфора и 17% кальция выводится организмом человека в виде растворов с мочой [15]. И очень малая часть от четырех металлов выводится с мочой в виде растворимых соединений: 1.4% медь; 1.6% железо; 0.81 % марганец и 3.6% цинк. (Можно ожидать, что у рыб будет аналогичная система выделения)
В. Мне хотелось бы, чтобы источником удобрений были только рыбы, но в моем аквариуме мало рыб. Стоит ли запустить их еще?
О. Нет. Можно просто сыпать в аквариум больше корма. Видите ли, рыбы сами по себе не вырабатывают питательные вещества. Они только перерабатывают то, что вы им даете в виде корма. Аэробные бактерии делают то же самое - расщепляют органику на питательные вещества, которые растения могут использовать.
Лично я сыплю корм в зависимости от объема аквариума, а не количества рыб в нем. Обычно даю больше корма, чем рыбы могут съесть, но не настолько, чтобы следующим утром можно было увидеть на дне гниющие остатки. Улитки очень помогают, потому что они расщепляют рыбий корм на более мелкие частицы, которые бактериям легче переработать.
***
В. Мне кажется забавным, что в последнее время в каждой статье о растениях говорится, что они не очень хорошо себя чувствуют без добавления в воду микроэлементов. Вы пытаетесь купить эти микроэлементы, но оказывается, что их или нет, или они слишком дорогие. Должен быть альтернативный способ снабдить аквариум железом и другими микроэлементами, не причинив рыбе вреда, есть ли такой?
О. Почва и корм для рыб.
Большинство "обычных" почв содержат огромные запасы железа и других микроэлементов. Кроме того в погруженной под воду почве создаются анаэробные условия, которые гарантируют доступность микроэлементов растениям.
Рыбий корм - совершенное удобрение. Не только потому, что содержит углерод и микроэлементы, но и потому, что оно относительно безопасно. Поскольку в результате обмена веществ рыб и бактерий, питательные вещества высвобождаются медленно и мелкими порциями, то для растений это больше подходит, чем внесение неорганических удобрений большими дозами раз в месяц или неделю. К тому же это дешевле.
На мой взгляд, если в аквариуме содержится не менее 2 мг/л (ppm) нитратов и слой почвы, то для растений должно быть достаточно питательных веществ. У аквариумиста должно сложиться представление о том, насколько часто нужно чистить аквариум. Ест ли смысл сначала удалять питательные вещества путем недокармливания рыб, подменами воды, чисткой грунта, а потом добавлять это все обратно в виде удобрений? (По мне, так это сизифов труд)
В. Понятия не имею, откуда вы взяли, что углерод из рыбьего корма превращается в CO2?Маловероятно, что углерод просто плавает в воде как чистый элемент. Углерод не означает СО2. Исходя из вашего предположения, мы могли бы просто засыпать в аквариум угля и ... тадам! - получим много СО2, но этого не происходит.
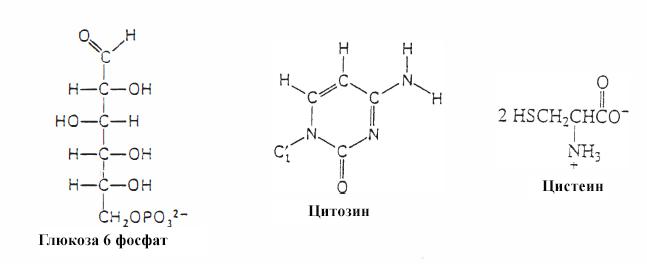
О. Углерод, из которого состоит древесный уголь, алмазы и графит, инертен. Организмы просто неспособны разорвать прочные углеродо-углеродные связи, из которых состоят эти соединения. Углерод, о котором я говорю, происходит из органического углерода в биомолекулах, из которых состоят организмы. Ниже приведены несколько примеров биомолекул - сахар, нуклеотид и аминокислота. Организмы легко превращают эти соединения в СО2.
С. Почва, как источник питательных веществ для растений.
Обычная почва - чрезвычайно концентрированный источник питательных веществ, особенно микроэлементов. Например, 10 кг обычной почвы обеспечат растениям моего экспериментального аквариума объемом 50 галлонов (190 л) запас железа на 330000 месяцев (таб. V-4). Даже если большая часть железа состоит в основном из нерастворимых оксидов железа, почва все равно должна обеспечивать растения железом до бесконечности.
таб. V-4
| химический элемент |
средняя концентрация |
запас питательных |
| B |
20 |
7700 |
| C |
20000 |
25 |
| Ca |
15000 |
2700 |
| Cu |
30 |
10000 |
| Fe |
40000 |
330000 |
| K |
14000 |
875 |
| Mg |
5000 |
2500 |
| Mn |
1000 |
125000 |
| Mo |
1.2 |
4000 |
| N |
2000 |
63 |
| P |
800 |
290 |
| S |
700 |
440 |
| Zn |
90 |
5600 |
Средняя концентрация элементов в почве взята у Боуэна (Bowen) [16]. Для подсчета запасов питательных веществ я использовала в качестве примера железо (Fe). Если килограмм сухой среднестатистической почвы содержит 40000 мг железа, то 10 кг почвы должны содержать 400000 мг железа. 400000 мг запасов, поделенные на необходимые растениям 1.2 мг ежемесячно, в результате дают 330000 мг - это сколько содержит почва месячного запаса железа. Концентрация железа (мг Fe на кг почвы), в зависимости от почвы находится в диапазоне от 2000 до 550000 [16]. Даже если я возьму 10 кг почвы с самым низким содержанием железа (2000 мг/кг), все равно моим растениям его хватит на 17000 месяцев.
Основных питательных веществ C, N и P в почве как раз не много. Кроме того, поступление питательных веществ из почвы, в отличие от корма для рыбы или воды, представляет собой ограниченный запас, который когда-нибудь да будет израсходован. Таким образом, хотя 25-месячный запас углерода и кажется не маленьким, он будет постепенно израсходован.
Большая часть углерода в почве находится в органической форме и при разложении выделяется в виде CO2. CO2 постепенно попадает в воду, где и усваивается растениями.
Чтобы рассчитать, как быстро будет высвобождаться углерод из почвы, я использовала скорость выброса СО2, равную 0,23 г СО2 в день на кг, описанную для одного из природных озерных грунтовых отложений [17]. Эти отложения содержали умеренное количество органического вещества (9,3%) и способствовали пышному росту водных растений. Используя эту скорость выброса CO2, я подсчитала, что 10 кг почвы в аквариуме выделяют 69г CO2 в месяц: 0.23 г CO2/кг грунтовых отложений/день * 10 кг субстрата * 30 дней/месяц = 69 г выход CO2 в месяц.
Углерод составляет 27.3% СО2. Таким образом, 69 г CO2 дают 18.8 г C, выделяемого в месяц. Если в килограмме среднестатистической почвы содержится 20000 мг углерода C (Таблица V-4), то общий его запас в 10 кг почвы в экспериментальном аквариуме составляет 200000 мг (200 г). Если C выделяется из почвы со скоростью 18,8 г в месяц, то почва будет обеспечивать растения углеродом примерно 11 месяцев (200 г + 18,8 г = 10,6 мес.).
В. У меня аквариум на 50 галл (200 л) и мне не везет с выращиванием в нем растений. В нем нет водорослей, а количество рыбьего населения в половину от рекомендованного. Грунт, толщиной почти 4 дюйма (10 см), который я регулярно сифоню во избежание высокого уровня аммиака. Растение сначала теряет старые листья, а потом в конце концов и само погибает. Не знаю, что не так. Освещение - две 30-ти ваттные люминесцентные лампы.
О. Похоже ваши растения голодают. Углерод составляет большую часть (около 40%) сухого веса растения. В таких аквариумах как мой (без дополнительного CO2) источником углерода является метаболизм рыб и бактерий (корм, остатки органики, питательная почва). Подозреваю, что ваш аквариум "слишком чист" для роста растений. (Отсутствие водорослей подтверждает гипотезу)
Почвенный слой очень важен для аквариума без дополнительного CO2, так как в процессе разложения органики почвы в воду в течение нескольких месяцев выделяется углекислый газ. Без почвы растения будут зависеть практически только от поступления углерода из корма рыб. Но должно пройти много времени, чтобы накопился сколь-нибудь значительный запас углерода из рыбьего корма. (Он будет либо растворен в воде, либо в виде иловых накоплений в грунте). Кроме того аквариумисты часто сами не дают скапливаться органическим веществам, постоянно вычищая от них аквариум - сифонят грунт, фильтруют воду угольным фильтром, удаляют протеин и прочее.
В вашем случае я либо довольствовалась только рыбами, либо переделала и перенастроила аквариум и для рыб и для растений. Этого можно добиться с помощью почвы, умеренной фильтрацией и редкими чистками. Смириться с "грязью" в аквариуме поможет вера в то, что растения смогут сами очистить его.
В. Я заметил, что растения в моем 70 галлонном (280 л) аквариуме с 5-ти летним торфяно-песчаным субстратом стали хуже расти. В эхинодорусах завелись зеленые нитчатые водоросли в виде пушистых комочков и тонких длинных зеленых нитей, обвивающих стебли растений.
Поначалу попробовал добавить карбонат кальция (CaC03) и пищевую соду (NaHC03). Гигрофила никак не отреагировала, но некоторые валлиснерии воскресли из мертвых и начали восстанавливаться. Затем я добавил английскую соль (MgS04), чтобы повысить концентрацию Mg и S, но безрезультатно.
Наконец, поставил бражку, чтобы добавить CO2. По видимому, CO2 был недостающим элементом. В течение 1 - 2 недель оклемалась гигрофила, донные растения пошли в рост, с Rotala macrandra тоже все стало хорошо. По вечерам все растения пузыряют кислородом. И рост водорослей, кажется также приостановился.
До этого аквариум годами обходился без дополнительного CO2. Быть может запасы углерода в грунте истощились?
О. Думаю, что вы правы в том, что рост растений в вашем аквариуме прекратился из-за постепенного истощения углерода в грунте. Первой подсказкой стало оживление валлиснерии после добавления CaC03 и NaHC03 - валлиснерия может использовать бикарбонат в качестве источника углерода.
Вероятно ваш торфяной субстрат не разлагался. С годами CO2, выделяющийся в результате разложения органики торфа, постепенно снижался. Судя по всему, вносимого рыбьего корма стало недостаточно для восполнения недостатка углерода в грунте.
Я подсчитала, что бактерии грунта высвободят 25-ти месячный запас углерода за 11 месяцев, но это сугубо теоретические расчеты, основанные на осадочных отложениях одного водоема. Высвобождение CO2 будет сильно различаться в зависимости от количества и типа органического вещества. Торф содержит много органических веществ, но он сильно кислый (pH 4-5), что препятствует разложению, тем самым значительно замедляя выделение CO2. Таким образом не удивительно, что в вашем случае высвобождение CO2 из песчано-торфяного субстрата заняло годы.
Вода, как источник питательных веществ
Около половины населения США, особенно те, кто живет в сельской местности, получают питьевую воду из подземных источников (общественные скважины и частные колодцы). Вторая половина, в основном горожане, получают воду из наземных водоемов - рек, водохранилищ. Такая вода проходит очистку.
Трудно делать какие-либо обобщения относительно уровня питательных веществ в питьевой воде, поскольку концентрации элементов сильно различаются в зависимости от источника воды (колодец против водохранилища), способа водоподготовки, металлических труб и т. д., а также от региональной географии. В любом случае, для данного региона вода из подземных источников скорее всего будет содержать больше питательных веществ, особенно Ca, Fe, K, Mg, Mn, S и Zn, чем городская вода. Более того, некоторые технологии очистки воды удаляют из нее тяжелые металлы, включая значительные количества Fe, Mn, Cu и Zn. В таблице V-5 приведены уровни питательных веществ, которые может содержать питьевая вода:
Таблица V-5
Химический
элемент
(ppm) | Грунтовые воды
(ppm) | Городской водопровод
(ppm) |
|---|
| среднее значение | диапазон | среднее значение | диапазон |
| B | - | - | 0.03 | 0.003 - 0.6 |
| C (в форме HCO3) | - | - | 9.0 | 0 - 75 |
| Ca | 36 | 0.5 - 230 | 26 | 0 - 145 |
| Cu | 0.004 | 0.1 - 3 | 0.008 | < 0.001 - 0.3 |
| Fe | 0.10 | 0.04 - 6000 | 0.02 | 0.005 - 0.1 |
| K | 2.4 | 0.5 - 4.0 | 1.6 | 0 - 30 |
| Mg | 12 | 0.2 - 70 | 6.3 | 0.0 - 120 |
| Mn | 0.05 | 0.1 - 110 | 0.003 | 0.001 - 0.01 |
| Mo | - | 0.4 - 40 | 0.001 | 0 - 0.07 |
| N | - | - | 0.1 | 0.08 - 1 |
| P | - | 0.1 - 10 | 0.02 | 0.01 - 0.2 |
| S | 22 | 0.1 - 10000 | 8.7 | 0 - 83 |
| Zn | 0.1 | 0.01 - 240 | 0.003 | 0.001 - 0.01 |
Что касается грунтовых вод, то я объединила данные исследования грунтовых вод США в 1984 году [18] с данными двух местных частных колодцев и отчетами об анализе грунтовых вод в двух крупных городах 1997 года. Для городской воды я объединила данные исследования 100 крупнейших городов США в 1962 году [18] и отчеты об анализе воды в нескольких крупных городах США за 1997 год.
Жесткость воды и "питательные вещества жесткой воды"
С технической точки зрения жесткость воды - это мера концентраций Ca и Mg в воде, причем Ca обычно преобладает.
Жесткость воды - это концентрация Ca и Mg, часто выражаемая как GH или ppm карбоната кальция (CaCO3). В природе жесткость воды обычно находится в прямой связи с pH, соленостью, удельной проводимостью и щелочностью.
Жесткость воды ничего не говорит о концентрациях бикарбонатов, Cl, K или S. Однако эти питательные вещества часто связаны с ней [19], поэтому жесткая вода часто содержит большое количество Ca, HC03-, Cl, K, Mg и S (т.е. "питательные вещества жесткой воды"). Однако это соотношение неверно для других питательных веществ N, P, Fe и Mn. Таким образом, городская питьевая вода из Портленда, которая довольно мягкая, содержит гораздо меньше основных питательных веществ, чем более жесткая вода Чикаго (Табл V-6).
Табл V-6
Параметры
(ppm) | Портланд | Чикаго |
|---|
Жесткость
(CaCO3) | 6.3 | 137 |
| HCO3- | 4.8 | 58 |
| Ca | 1.6 | 36 |
| Cl | 1.0 | 13 |
| K | 0.2 | 1.5 |
| Mg | 0.6 | 11 |
| S | < 0.2 | 9.7 |
Я добавляла по 40 л воды в экспериментальный аквариум каждый месяц. В Табл V-7 показано гипотетическое поступление питательных веществ с доливом воды в экспериментальный аквариум. Жесткость воды будет иметь решающее значение для обеспечения растений основными питательными веществами Ca, Mg, K и S.
Поскольку расчеты "запаса питательных веществ" основывались на средних значениях, то растения в мягкой воде получали бы меньше питательных веществ, а в некоторых случаях, возможно, и недостаточно.
Я бы предостерегла аквариумистов от бездумного использования уровня жесткости воды для классификации их водопроводной воды. Жесткость - это жесткость, а не pH и щелочность. Хотя все три параметра часто коррелируют в природе, в условиях искусственной водопроводной воды такого может не быть. Возможно это связано с тем, что муниципальный водоканал может добавлять бикарбонаты в кислую мягкую воду для предотвращения коррозии металлических труб. Такая вода с ее искусственной щелочностью все равно является «мягкой водой» и, следовательно, в ней не хватает многих питательных веществ, необходимых для растений, живущих в жесткой воде (например, Ca, Mg, K и S).
Табл V-7
Химический
элемент | Концентрация
(мг/л) | Запас
питательных
веществ
(месяцев) |
|---|
| B | 0.03 | 46 |
| C | 9 | 0.05 |
| Ca | 31 | 22 |
| Cu | 0.006 | 8 |
| Fe | 0.06 | 2 |
| K | 2 | 0.5 |
| Mg | 9 | 18 |
| Mn | 0.03 | 15 |
| Mo | 0.001 | 13 |
| N | 0.1 | 0.01 |
| P | 0.02 | 0.03 |
| S | 15 | 38 |
| Zn | 0.05 | 13 |
Для расчета концентрации элементов я использовала средние значения из Табл V-5. Расчет запаса питательных веществ продемонстрирую на примере K (калий). Поскольку питьевая вода содержит около 2 мг/л K (Таблица V-5), 40 литров добавленной воды будут содержать 80 мг K. Растениям в экспериментальном аквариуме требуется 160 мг/месяц калия (см. Таблицу V-1). Ежемесячное внесение 80 мг калия с доливом воды, поделенное на 160 мг, необходимые растениям, дает запас калия на пол месяца.
В. В моем 100 галл (380 л) аквариуме с радужницами, на листьях амазонского эхинодоруса появляются дырки, а затем листья просто разрушаются. Грешу на недостаток света. Вода мягкая, в качестве грунта гравий. Что может быть?
О. Растения могут страдать от дефицита одного из питательных веществ жесткой воды. В мягкой воде почти всегда не хватает K, Ca и Mg. Амазонские эхинодорусы - прожорливые растения, им необходимо много питательных веществ. Считается, что они не подходят для аквариумов с мягкой водой, т.е. с водой, у которой GH < 4 и/или жесткостью менее 60 ppm CaCO3.
Что касается кальция - то можно добавить CaCO3. Один любитель регулярно добавляет в свой аквариум объемом 70 галл (265 л) кальциевую биологически активную добавку (БАД) из аптеки. Для магния - английская соль, которая не что иное, как MgSO4·7H2O.
Не смотря на то, что Ca и Mg относительно безвредны, при внесении добавок стоит контролировать жесткость воды. Аквариумные тесты для проверки жесткости не дороги и доступны. Также можно положить в фильтр мешочек с доломитовым гравием. (Мешочки можно сделать из женских колготок). Чтобы обеспечить растения калием, можно использовать удобрения или заменитель соли из продуктового магазина (оба являются KCl). Если вы добавите щепотку (или примерно 1/8 чайной ложки) на каждые 10 галлонов (38 л), у вас должно получиться 10 ppm K, что вполне достаточно. [При расчете дозировки KCl обратите внимание, что 1 чайная ложка KCl весит около 5 г. (или 5000 мг), и примерно половина веса составляет Cl.]
Ответ: Я добавил устричную крошку из фермерского магазина в фильтры и субстрат аквариума. С "амазонками" теперь все в порядке.
Доступность питательных веществ растениям в аквариуме
Таблица V-8 суммирует все данные, представленные ранее, путем сравнения снабжения растений питательными веществами в экспериментальном аквариуме объемом 50 галлонов (190 л) из корма для рыб, из почвы и из воды.
Табл V-8
Химический
элемент | Запас питательных веществ (месяцев)
из: |
|---|
| корм для рыб | почва | вода |
| B | 40 | 7700 | 46 |
| C | 2 | 25 | 0.05 |
| Ca | 14 | 2700 | 22 |
| Cu | 36 | 10000 | 8 |
| Fe | 9 | 330000 | 2 |
| K | 3 | 875 | 0.5 |
| Mg | 5 | 2500 | 18 |
| Mn | 80 | 125000 | 18 |
| Mo | 9 | 4000 | 13 |
| N | 10 | 63 | 0.01 |
| P | 19 | 290 | 0.03 |
| S | 14 | 440 | 38 |
| Zn | 30 | 5600 | 13 |
Запас питательных веществ из рыбьего корма, почвы и воды был взят из таблиц, приведенных в других главах книги.
Видимо, мои опасения по поводу дефицита питательных микроэлементов были излишними. Как видим, почва в экспериментальном аквариуме содержит массу питательных веществ, включая огромный запас железа. Редкий легкий хлороз, который я наблюдала у своих растений, вероятно, был вызван не дефицитом железа, а другими факторами, такими как аллелопатия и токсичность металлов.
Вероятно углерод является ограничивающим питательным веществом для роста погруженных аквариумных растений, так как его мало во всех источниках питательных веществ.
У растений в прудах будет меньше шанс испытать дефицит углерода, так как они получают углерод не только из рыбьего корма, почвы и воды. Например, жуки, опавшие листья и прочая падающая в пруд органика содержат углерод. Кроме того, в прудах обычно растут кувшинки и другие надводные растения. Такие растения поставляют углерод в воду из воздуха. Они накапливают углерод из воздуха в результате фотосинтеза, и когда их листья отмирают, то накопленный углерод освобождается и становится доступным погруженным растениям.
Литература
1. Peverly JH. 1979. Elemental distribution and macrophyte growlth downstrearn from an organic soil.
Aquat. Bot. 7: 319-338.
2. Sposito G. 1986. Distribution of potentially hazardous trace metals. In: Sigel H (ed), Metal Ions in
Biological Systems (Vol 20). Marcel Dekker (N'Y), pp 1-20.
3. Davies BE and Jones LHP. 1988. Micronutrients and toxic elements. In: Wild A (ed), Russell's Soil
Conditions and Plant Growth (11th Edition). John Wiley (NY), pp. 780-814.
4 Bowen HJM 1979. Environmental Chemistry of the Elements. Academic Press (N'Y), pp. 132-133.
5. Bowen 1979, p. 69.
6. Martin RB. 1986. Bioinorganic chemistry of metal ion toxicity. In: Sigel H (ed), Metal Ions in Biological
Systems (Vol 20). Marcel Dekker (N'Y), pp. 21-45.
7. Tacon AGJ and DeSilva SS. 1983. Mineral composition of some commercial fish feeds available in
Europe. Aquaculture 31: 11-20.
8. Crawford DL and Law DK. 1972. Mineral composition of Oregon pellet production formulations.
Prog. Fish-Cult. 34: 126-130.
9. NAS. 1977. Nutrient Requirements of Warnwater Fishes. National Academy of Sciences (Washington,
DC).
10. Bowen 1979, Table 6.3.
11. Bowen 1979, Table 6.2.
12. Bengston DA, Beck AD and Simpson KL. 1985. Standardization of the nutrition of fish in aquatic
toxicological testing. In: Mackie AIVI and Bell JG (eds). Nutrition and Feeding in Fish. Academic
Press (NY), pp 431-445.
13. Tarifeno-Silva E, Kawasaki LY, Yu DP, Gordon MS and Chapman DJ. 1982. Aquacultural approaches
to recycling of dissolved nutrients in secondarily treated domestic wastewaters- III. Uptake of
dissolved heavy metals by artificial food chains. Water Res. 16: 59-65.
14. Mertz W (ed.). 1987. Trace Elements in Human and Animal Nutrition- Fifth Ed. Vol. 1. Academic
Press (N'Y).
15. Bowen 1979, Table7.6.
16. Bowen 1979, Table 4.4.'
17. Barko JW and Smart R.\1. 1983. Effects of organic matter additions to sediment on the growth of
aquatic plants. J. Ecol. 71: 161-175.
18. van der Leeden F, Troise FL, and Todd DK. 1990. The Water Encyclopedia, Second Ed., Lewis
Publishers (Boca Raton LA).
19. Wetzel RG. 1983. Limnology (Second Ed.). Saunders College Publishing (Philadelphia, PA), p. 179-
201.






***
Комментарии: